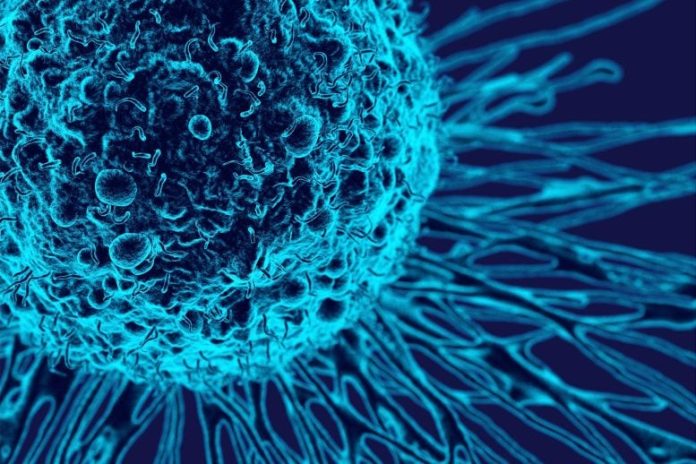
La ricerca sul cancro ha compiuto un nuovo passo avanti, offrendo una speranza concreta per milioni di pazienti. Un team di ricercatori della Perelman School of Medicine presso l’Università della Pennsylvania ha messo a punto una strategia innovativa che potrebbe rivoluzionare il trattamento di numerosi tipi di tumore. Questa nuova terapia si basa sull’utilizzo di piccole vescicole extracellulari (sEV), minuscole capsule ingegnerizzate da cellule umane, in grado di attivare un meccanismo di autodistruzione nelle cellule tumorali.
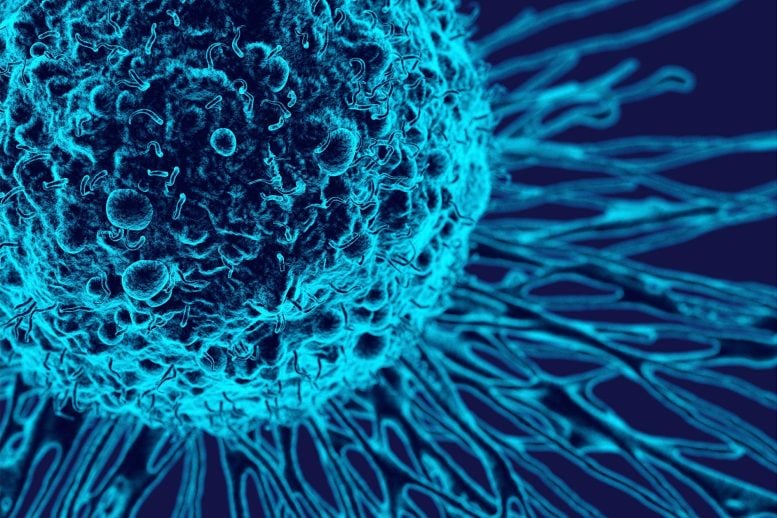
Le vescicole extracellulari come nuova frontiera nella lotta al cancro
Al centro di questa scoperta c’è il recettore DR5, una proteina presente sulla superficie di molte cellule tumorali. Quando attivato, DR5 induce un processo di autodistruzione cellulare noto come apoptosi. Nonostante decenni di ricerca, sviluppare terapie efficaci che colpiscano specificamente DR5 è sempre stato un obiettivo sfuggente.
Gli scienziati hanno ingegnerizzato le sEV in modo che possano legarsi specificamente a DR5. Una volta a contatto con la cellula tumorale, le sEV attivano il recettore, innescando il processo di apoptosi. I risultati ottenuti sono stati sorprendenti: le sEV si sono dimostrate più efficaci degli anticorpi, precedentemente considerati la strategia più promettente per targeting DR5. Nei test in vitro, le sEV hanno eliminato con successo numerosi tipi di cellule tumorali, mentre nei modelli murini hanno bloccato la crescita del cancro e prolungato significativamente la sopravvivenza degli animali.
Questa innovativa strategia terapeutica, basata sull’utilizzo di sEV, presenta numerosi vantaggi rispetto alle terapie convenzionali. La capacità delle sEV di colpire in modo selettivo le cellule tumorali, unita alla loro maggiore efficacia nel targeting di DR5, apre nuove prospettive per lo sviluppo di trattamenti più personalizzati e meno invasivi. La versatilità di questa tecnica suggerisce un ampio spettro di applicazioni cliniche, rendendola una promettente candidata per la terapia di diversi tipi di cancro.
I risultati ottenuti in questa fase preclinica sono estremamente promettenti e aprono la strada a nuove sperimentazioni cliniche sull’uomo. Gli autori dello studio hanno evidenziato l’importanza di continuare a investire nella ricerca sulle terapie cellulari, in particolare per i tumori solidi, dove le attuali immunoterapie non sono sempre efficaci.
Il bersaglio: il recettore della morte 5 (DR5)
Il professor Xiaowei Xu, figura di spicco nella ricerca sul cancro presso la Penn Medicine, ha sottolineato come questa nuova strategia rappresenti un significativo passo avanti nella lotta contro il cancro: “Abbiamo ottenuto risultati molto promettenti in laboratorio“, ha affermato: “E siamo entusiasti di poter portare questa terapia innovativa in clinica. Nonostante i progressi fatti nell’immunoterapia, sappiamo che c’è ancora molto margine di miglioramento, soprattutto per i tumori solidi come il melanoma. Questa nuova strategia ci offre una speranza concreta per i pazienti che non rispondono alle terapie convenzionali“.
Il recettore DR5, evolutosi per eliminare le cellule danneggiate, si è rivelato un bersaglio promettente nella lotta contro il cancro. Tuttavia, nonostante i numerosi tentativi, i trattamenti finora sviluppati non sono riusciti a sfruttare appieno il potenziale di questo recettore. Il team del professor Xu ha adottato un approccio innovativo, utilizzando vescicole extracellulari – minuscole capsule prodotte naturalmente dalle cellule – per attivare selettivamente DR5. Questa strategia si basa sull’intrinseca capacità delle vescicole di comunicare tra le cellule, offrendo una nuova prospettiva nella terapia oncologica.
Gli scienziati del team hanno utilizzato sEV derivate da cellule NK, cellule immunitarie note per la loro capacità di uccidere le cellule tumorali. Queste vescicole, agendo come dei ‘pacchetti’ molecolari, sono state modificate per trasportare un frammento di anticorpo in grado di attivare il recettore DR5 sulle cellule tumorali. In questo modo, le sEV NK diventano dei veri e propri missili guidati, capaci di individuare e distruggere selettivamente le cellule malate.
Le sEV si sono rivelate altamente specifiche nel targeting del recettore DR5, legandosi a esso e innescando un meccanismo di autodistruzione nelle cellule tumorali. Questa azione è stata particolarmente efficace nei confronti di tumori con un’elevata espressione di DR5, come il melanoma, il carcinoma epatocellulare e il carcinoma ovarico. In modelli animali, il trattamento con sEV ha portato a una significativa riduzione del volume tumorale e a un prolungamento della sopravvivenza.
Gli esperimenti condotti dal team di Xu hanno rivelato un’azione sinergica degli sEV nel microambiente tumorale. Oltre a eliminare le cellule tumorali, gli sEV hanno attaccato anche altre cellule coinvolte nella progressione tumorale, come i fibroblasti associati al cancro e le cellule mieloidi soppressive. Inoltre, hanno stimolato l’attività delle cellule T, contribuendo a creare un ambiente tumorale più favorevole alla risposta immunitaria. Questa capacità multifunzionale rende gli sEV una promettente strategia terapeutica per i tumori solidi, dove l’ambiente tumorale è spesso altamente soppressivo.
Conclusioni
I ricercatori hanno dimostrato la fattibilità di produrre gli sEV su larga scala e di conservarli per lunghi periodi, rendendoli una promettente opzione terapeutica contro il cancro. I prossimi passi includeranno l’ottimizzazione dei processi produttivi per ottenere sEV di alta qualità e la conduzione di studi preclinici approfonditi per valutarne la sicurezza e l’efficacia in vista delle sperimentazioni cliniche sull’uomo.
Lo studio è stato pubblicato su Science Advances.